Osimertinib dose-reduction and survival in 1L EGFR-mutated metastatic non-small cell lung cancer (mNSCLC). Adam Barsouk et al. Lung Cancer, 2026.
オシメルチニブはEGFR変異陽性肺癌の一次治療として広く用いられていますが、皮膚障害や下痢などの副作用により、「減量すべきかどうか」に悩む場面は少なくありませんね。
一方で、減量によって治療効果、すなわちPFSや、とくに中枢神経(CNS)病変のコントロールが損なわれないのか、さらにOSへどのような影響があるのか、不安を感じることも多いと思います。
本稿では、一次治療としてオシメルチニブを使用した実臨床データを報告した論文に基づき、減量という選択を日常診療でどのように考えるべきかを整理してみます。
This is an open access article under the CC BY license
はじめに

一次治療のEGFR変異陽性NSCLCではオシメルチニブが標準になっていますが、実臨床では皮膚障害や下痢、肺障害などで「減量せざるを得ない」場面が出てきますよね。
実際、FLAURAでも重篤な有害事象や休薬、減量が一定数ありました

ところが、「減量しても効果は保てるのか」「むしろ副作用が減って治療継続できて良いのか」は研究によって結果が割れており、そこがモヤモヤポイントなんですね。
この研究は、一次治療でのオシメルチニブ減量(80mg→40 mg)が、無増悪生存期間(PFS)や全生存期間(OS)にどう影響するかを、実臨床データで比較したものです。
背景
FLAURA試験以降、オシメルチニブは一次治療のEGFR変異(mt)転移性NSCLCの標準治療となった。
しかし、オシメルチニブの減量が、通常量と比べて転帰に与える影響に関するデータは限られている。
方法と目的
2018年から2023年に一次治療としてオシメルチニブを受けたEGFR変異転移性NSCLC患者を対象に、単施設の後ろ向き解析を行った。
減量を行った患者と、通常量(80 mg/日)を維持した患者を比較した。
背景因子、疾患特性、治療歴、有害事象、臨床転帰を電子カルテから抽出し、独立標本t検定やカイ二乗検定で比較した。
- 無増悪生存期間(mPFS)
- 中止までの期間(mTTD)
- 全生存期間(mOS)
をKaplan–Meierのlog-rank検定および時間変動共変量を用いたCox回帰で比較した。
結果
一次治療でオシメルチニブを受けた171例のうち、26例(15%)で減量が必要であった。
性別、人種、診断時ECOG PS>1、喫煙歴は減量群と通常量群で同程度。
診断時の中枢神経(CNS)転移は減量群44%、通常量群34%。
減量群は全例が有害事象を経験したのに対し、通常量群では48%であった。
減量群は通常量群よりmPFSが短かった(17.0か月 vs 24.6か月)。
CNS転移がある患者でもない患者でも、減量後のPFSは通常量より短かった。
時間変動を用いた多変量解析でも、減量は背景因子にかかわらずPFS不良と関連した。
TTDは同程度であり(21.3か月 vs 25.2か月)、OSも同程度であった(36.7か月 vs 39.2か月)。
有害事象でオシメルチニブを中止した患者は14例(8%)で、そのうち9例(64%)は以前に減量されていた。
中止群と非中止群でmPFSとmOSは同程度であった。
結語
オシメルチニブ減量は比較的まれであり、(主としてCNS進行による)PFS短縮と関連したが、TTDとOSは一次治療のEGFR変異転移性NSCLCで同程度であった。

感想です。
どんな結果だった?
研究デザインの要点
- 単施設・後ろ向き
- 対象:2018/5/1〜2023/5/1に一次治療オシメルチニブを受けたEGFR変異mNSCLC 171例(化学療法先行や併用は除外)PIIS0169500226000310
- 比較:減量群 vs 80 mg維持群(減量は時間変動共変量として解析)
患者背景
背景因子(性別、人種、ECOG、喫煙など)は概ね同等。
診断時CNS転移は減量群の方がやや多いですが有意差はついていません(44% vs 34%:P=0.192)。
PFSとCNS
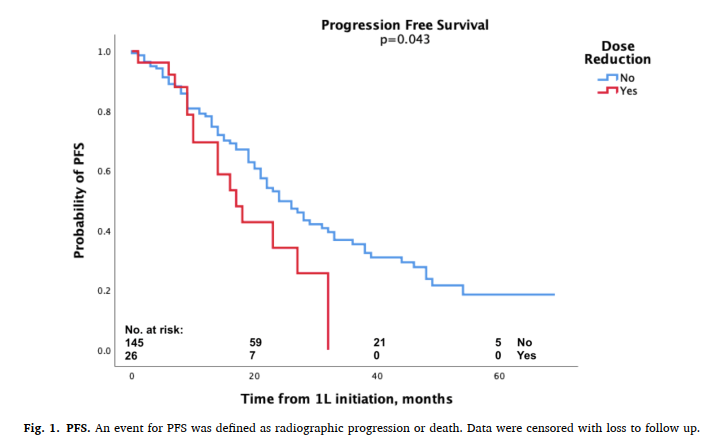
- mPFS:減量群 17.0か月 vs 維持群 24.6か月(p=0.043)
- CNSでの進行割合:減量群 69% vs 維持群 32%(p<0.001)
- (ベースラインCNS転移なしの集団で)CNS進行までの期間:減量群 15.7か月 vs 維持群 23.4か月(p=0.039)
多変量解析(時間変動共変量)
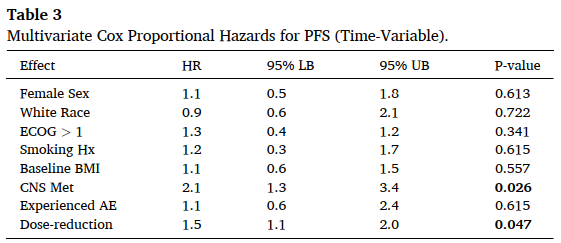
- 減量はPFS不良と関連(HR 1.5、p=0.047)
- 併せて、ベースラインCNS転移もPFS不良と関連(HR 2.1、p=0.026)
TTD / OS
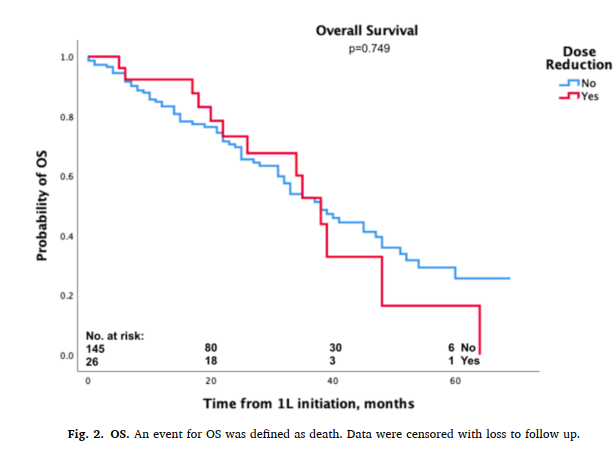
- mTTD:21.3 vs 25.2か月(有意差なし)
- mOS:36.7 vs 39.2か月(有意差なし)
まとめ
| 項目 | 減量群 (n=26) | 維持群 (n=145) | ざっくり解釈 |
|---|---|---|---|
| mPFS | 17.0か月 | 24.6か月 | 減量でPFS短い |
| CNS進行割合 | 69% | 32% | 減量群でCNS進行が目立つ |
| CNS進行まで(CNSなし集団) | 15.7か月 | 23.4か月 | CNS制御が弱い可能性 |
| mTTD | 21.3か月 | 25.2か月 | 治療継続期間は同程度 |
| mOS | 36.7か月 | 39.2か月 | OSは同程度 |
論文解釈に注意するポイント
この研究のメッセージはシンプルで、減量はPFSを短くしうるが、OSとTTDは大きく変わらないという結果でした。
一方で、著者らは「既報の多く(特に高齢集団を含む研究)では、減量群のPFSがむしろ良い/長い」と報告されてきた点も整理しています。今回の研究は中央値年齢が約62–63歳で、先行研究(中央値75歳)との患者背景の違いが影響した可能性がある、という説明ですね。
さらに重要なのがCNSです。今回、減量群のPFS短縮は「主にCNS進行」で説明されうる、と議論しています。
著者らは、オシメルチニブの血液脳関門移行や、減量では脳転移抑制の非劣性を示せない可能性を背景として挙げています。
注意点 リミテーション
- 後ろ向き研究であること、減量群が少ない(n=26)
- PFSの後ろ向き評価はバイアスを受けやすい
- AE対応や減量判断に医師・患者間のばらつきがあり、未測定の交絡が残りうる
- 減量群でベースラインCNS病変が多い傾向があり、PFS不利に寄与しうる
まとめ:臨床現場でどう活かす?
- 減量はPFSを悪化させるが、OSを必ずしも悪化させない可能性がある。
- 減量後の増悪は、二次治療で挽回可能?
- CNS制御は弱くなるかもしれない
という感じでしょうか。
例1:皮膚障害/下痢でQOLが低下している患者
本研究ではTTDやOSに有意差が認められなかったことから、症状が強い場合には減量は現実的な選択肢になり得ますね。
一方で、CNS進行リスクが示唆されている点には注意が必要で、全身症状の改善とCNS制御のバランスを意識しながら判断することが重要になりそうです。
例2:すでに脳転移がある/既往がある患者
この集団では、より慎重な判断が求められますね。減量群ではCNS進行が多く、CNS進行までの期間も短いという所見が示されています。
症状や画像所見を踏まえつつ、局所治療の併用も視野に入れながら、CNSモニタリングを厚めに行うべきかを検討する場面と言えそうです。

<スマートフォンをご利用の皆さまへ>
他の記事をご覧になりたい場合は、画面下の「メニュー」「検索」「サイドバー」を使って、気になる話題を検索することもできますので、ぜひご活用ください。
<PCをご利用の皆さまへ>
他の記事をご覧になりたい場合は、画面上部のメニューバーや画面右側のサイドバーをご利用いただき、気になる話題をお探しください。

