「発熱や倦怠感が続く高齢の患者さんが多いけど、なかなか診断がつかない……」
「肺に間質性肺疾患っぽい所見があって、腎機能が悪い‥‥」
そんなとき、頭の片隅に「血管炎」は浮かんでいますか?
ちなみに、診断に重要なのは「生検」です(正拳ではない・・・)。
顕微鏡的多発血管炎(microscopic polyangiitis: MPA)は、見逃すと命に関わるが、診断すれば治療可能な疾患です。
今回の記事では、臨床の現場で役立てられる視点から、MPAのイメージがつかめるようにざっくり解説していきます。
参考:ANCA関連血管炎診療ガイドライン2023
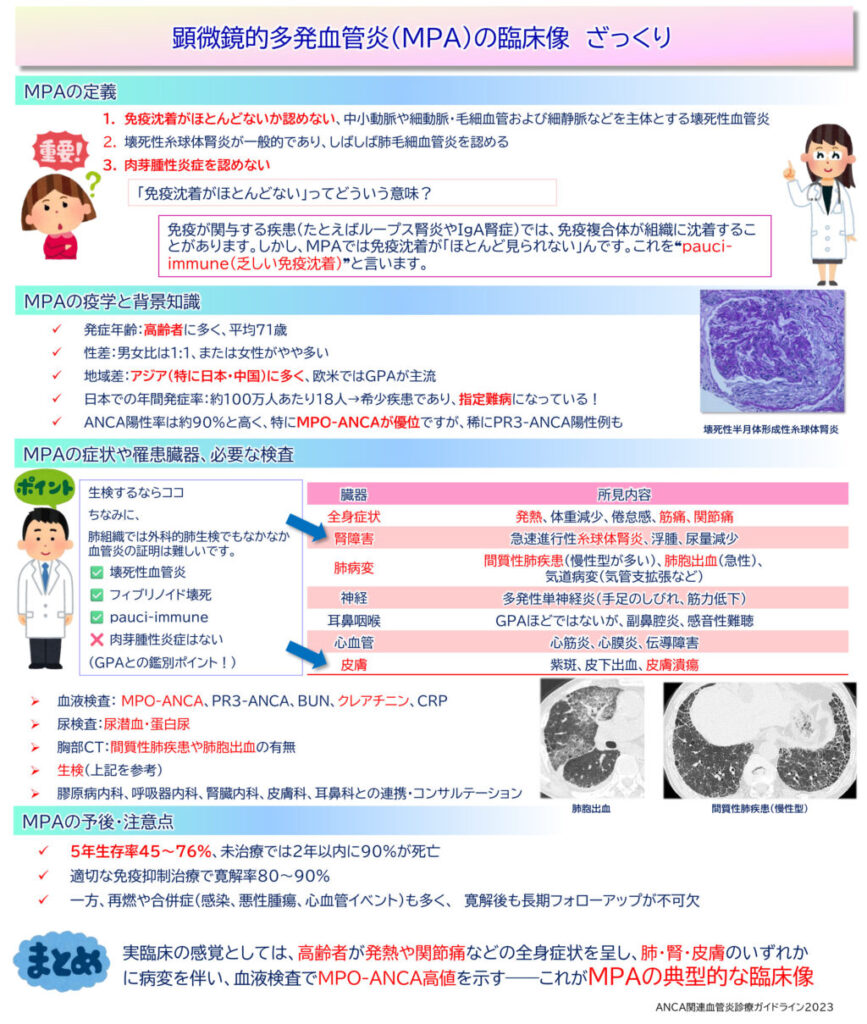
MPAとは?(定義と分類)
MPAは、ANCA関連血管炎(AAV)の1つで、主に毛細血管、細動脈、細静脈といった小型血管に炎症を起こす壊死性血管炎です。
定義
- 免疫沈着がほとんどないか認めない、中小動脈や細動脈・毛細血管および細静脈などを主体とする壊死性血管炎
- 壊死性糸球体腎炎が一般的であり、しばしば肺毛細血管炎を認める
- 肉芽腫性炎症を認めない
「免疫沈着がほとんどない」ってどういう意味?
通常、免疫が関与する疾患(たとえばループス腎炎やIgA腎症)では、免疫複合体(抗原と抗体のかたまり)が組織に沈着し、それが炎症を引き起こします。
しかし、MPAではこの免疫沈着が「ほとんど見られない」んです。
これを医学的には:
❝pauci-immune(ポウシ・イミューン=乏しい免疫沈着)❞
と呼びます。
つまり、免疫染色(免疫蛍光染色)でほとんど光らない=免疫沈着が乏しい=ANCAが主役の炎症ということです。
「中小動脈・毛細血管・細静脈などを主体とする壊死性血管炎」って?
血管炎は、「どの大きさの血管に炎症が起きるか」で分類されます。MPAは:
✅ 中型~小型血管(中小動脈・細動脈・毛細血管・細静脈)を中心に
✅ 壊死性=血管が壊れて死んでしまうような強い炎症
が起きます。
つまり、腎臓の糸球体(毛細血管のかたまり)や肺の毛細血管にダメージを与えるタイプの血管炎です。
「壊死性糸球体腎炎が一般的」って?
「糸球体」とは、腎臓で血液をろ過するフィルターのような構造。MPAではここに炎症が起きて、
❝壊死性糸球体腎炎(rapidly progressive glomerulonephritis: RPGN)❞
を引き起こします。これは、尿所見では血尿や蛋白尿、血液検査ではクレアチニン上昇として現れ、短期間で腎不全に進行することもあります。
「しばしば肺毛細血管炎を認める」って?
肺の中にも毛細血管がびっしり張り巡らされています。ここにも同じく血管炎が起きると、血液が漏れ出して:
✅ 肺胞出血(血痰、喀血、呼吸困難)
といった命に関わる症状を引き起こします。
この腎障害+肺障害のセットは、MPAの典型的なパターンの一つです。
「肉芽腫性炎症を認めない」ってどういうこと?
「肉芽腫性炎症」とは、異物や慢性炎症に対してできる特殊な炎症組織のことで、結核やサルコイドーシス、GPAなどで見られる病理所見です。
🔴 GPA(多発血管炎性肉芽腫症)にはこれが特徴的に見られますが、
🔵 MPAには肉芽腫性炎症は基本的に「見られません」。→ここ重要!!
つまり:
病理学的に「壊死性血管炎はあるけど、肉芽腫はない」→ MPAの大きな診断ポイント!
疫学と背景知識
- 発症年齢:高齢者に多く、平均71歳
- 性差:男女比は1:1または女性がやや多い
- 地域差:アジア(特に日本・中国)に多く、欧米ではGPAが主流
- 日本での年間発症率:約100万人あたり18人
ANCA陽性率は約90%と高く、特にMPO-ANCAが優位ですが、稀にPR3-ANCA陽性例もいます。
✔ MPAの特徴
| 項目 | 内容 |
|---|---|
| 炎症部位 | 小型血管(腎糸球体、肺毛細血管など) |
| ANCA | 主に MPO-ANCA(p-ANCAパターン)陽性 |
| 肉芽腫形成 | なし(GPAとの鑑別点) |
| 主な臓器障害 | 腎、肺、神経、皮膚、心臓など |
| 鑑別が必要な疾患 | GPA、EGPA、腎限局型血管炎 |
症状は?(臨床像)
MPAは多臓器性疾患です。典型的な臓器障害を臓器別に分類すると以下のようになります:
🔴 全身症状
- 発熱、体重減少、倦怠感、筋痛、関節痛(非特異的)
- 数週間〜数ヶ月かけて徐々に進行することが多い
🧪 腎障害(最も多い) 重要
- 急速進行性糸球体腎炎(RPGN)
- 血尿・蛋白尿・円柱尿 → 数週間で腎不全に進行する例も
- クレアチニン上昇、浮腫、尿量減少など
🫁 肺病変 重要
- 間質性肺炎(ILD)(UIPパターンが多い)
- 肺胞出血(DAH):喀血、血痰、呼吸困難、酸素化不良など
- 気道病変:気管支拡張や慢性気管支炎など
🧠 神経
- 多発性単神経炎(手足のしびれ、筋力低下)
- 一部は治療後も後遺障害が残る
👂 ENT(耳鼻咽喉)
- GPAほどではないが、副鼻腔炎、感音性難聴などが出現しうる
🫀 心血管
- 心筋炎、心膜炎、伝導障害など
- 心電図異常(QT延長、房細動など)と関連
🟤 皮膚 重要
- 紫斑、皮下出血、皮膚潰瘍などが見られる
- 病理では小血管の壊死性血管炎を認めることがあり、皮膚生検は低侵襲で診断に有用
診断の進め方(基本フロー)
MPAの診断は複数の検査を組み合わせて行う必要があります:
1. 血液検査
- ANCA(主にMPO-ANCA)陽性(約60〜70%)
- CRP、白血球増多、赤沈亢進などの炎症反応
- 腎機能(Cre、BUN)チェック
2. 尿検査
- 血尿・蛋白尿・赤血球円柱
尿沈渣・尿定性検査をチェックするクセをつけましょう。
3. 画像検査
- 胸部CT:ILDや肺胞出血の所見
- 副鼻腔CT
4. 生検(可能なら必須!)
| 生検部位 | 特徴・診断率 | コメント |
|---|---|---|
| 腎臓 | 最も診断率が高い | 腎障害がある場合は腎生検が第一選択だが、腎機能が正常でも壊死性糸球体腎炎の所見が認められることがある |
| 皮膚 | 中等度の診断率 | 紫斑や潰瘍の部位には血管炎の所見が認められることがあり、体表からの生検で侵襲が少なく実施しやすいため、診断目的として有用 |
| 末梢神経 | やや低め | 単神経炎の患者で神経筋生検が有効なことも |
| 肺(経気管支・外科的) | 難易度高 | 肺胞出血や間質性陰影がある場合に検討。ただし、経験的には外科的肺生検でも診断的な所見が得られないことが多い。TBLBで確定診断に至った例は、個人的には見たことがありません。リスクに対して得られるベネフィットは非常に乏しい。 |
| 筋肉 | 有効な場合あり | 神経とセットで「筋・神経生検」として行われることも |
生検組織で見るべき特徴は以下です:
✅ 壊死性血管炎(血管の壁が壊れている)
✅ フィブリノイド壊死(血管の中が“とろけたよう”に見える)
✅ 免疫沈着が乏しい(pauci-immune)
❌ 肉芽腫性炎症はない(GPAとの鑑別ポイント!)
特に腎生検では、壊死性半月体形成性糸球体腎炎(crescentic GN)を確認できれば、MPAと診断する決め手になります。
ざっくり治療戦略(寛解導入→維持)
本記事では、治療の全体像をざっくりご紹介します。詳細な治療方針や薬剤選択については、別記事であらためて解説予定です。
日本の「ANCA関連血管炎 診療ガイドライン2023」では、MPAとGPAに対してほぼ共通のレジメンが提案されています。主な選択肢は以下の通りです:
▶ 寛解導入療法
1.グルココルチコイド+シクロフォスファミド(CY)
- 経口より静注の方が推奨度高
2.グルココルチコイド+リツキシマブ(RTX)
- 高齢者や再発例、CY使用が難しい場合に有用
3.重症臓器病変なし+腎機能障害が軽度
→ グルココルチコイド+メトトレキサート
4.重症臓器病変あり or 腎機能障害が中等度以上
→ グルココルチコイド+ミコフェノール酸モフェチル(セルセプト)
5.アバコパン(タブネオス)併用レジメン
- CYまたはRTXと併用し、グルココルチコイドの代替または減量目的で使用可能
▶ 寛解維持療法
- 維持療法の目的は「再燃防止」と「副作用最小化」
- 主な薬剤:リツキシマブ、アザチオプリン、メトトレキサート
- 少なくとも1〜2年は継続が必要
予後と注意点
- 5年生存率45~76%
- 未治療では2年以内に90%が死亡
- 適切な免疫抑制治療で寛解率80〜90%
- 一方、再燃や合併症(感染、悪性腫瘍、心血管イベント)も多く、
寛解後も長期フォローアップが不可欠
📌 感染症は重篤合併症の約30%を占め、
呼吸器感染症が最多(特にステロイド大量使用中)
🎓最後にひとこと
実臨床の感覚としては、高齢者が発熱や関節痛などの全身症状を呈し、肺・腎・皮膚のいずれかに病変を伴い、血液検査でMPO-ANCA高値を示す――これがMPAの典型的な臨床像であると感じます。
今回のブログの内容を参考に、ぜひ、明日の診療に活かしてください!

<スマートフォンをご利用の皆さまへ>
他の記事をご覧になりたい場合は、画面下の「メニュー」「検索」「サイドバー」を使って、気になる話題を検索することもできますので、ぜひご活用ください。
<PCをご利用の皆さまへ>
他の記事をご覧になりたい場合は、画面上部のメニューバーや画面右側のサイドバーをご利用いただき、気になる話題をお探しください。

