Checkpoint inhibitor effectiveness after corticosteroids and second-line immunosuppressants for immune-related adverse events in non-small-cell lung cancer. van Dijk et al. ESMO Open, 2026.
免疫チェックポイント阻害薬(ICI)治療中に起こる免疫関連有害事象(irAE)は、しばしば高用量ステロイドによる治療を要します。
しかし、その免疫抑制が「ICIの抗腫瘍効果を弱めているのではないか?」という疑問を、私たちはどこまで真剣に考えているでしょうか。
本稿では、NSCLCにおけるirAE治療後のステロイド量とICI有効性の関係を検討した最新研究を、臨床目線で読み解きます。
This is an open access article under the CC BY license
はじめに

ICIは進行NSCLCの標準治療になりましたが、免疫が過剰に働くことでirAEが起こりえます。
重症(一般にGrade ≥3)のirAEでは高用量ステロイド(例:1–2 mg/kg相当)が提案され、反応が悪い場合は免疫抑制薬も使います。

ただし最近、「強い免疫抑制=ICIの抗腫瘍効果を弱めて生存を悪化させるかも」という懸念が出ています。
これまでのデータはメラノーマ中心で、NSCLCでは十分な規模で検証されていませんでした。
そこで本研究は、世界規模の実臨床コホートで、ステロイド“最大投与量”と“累積投与量”を分けて、さらに免疫抑制薬も含めて、生存との関連を見にいった、という位置づけです。
背景
近年の研究により、免疫チェックポイント阻害薬(ICI)治療中に発生した免疫関連有害事象(irAE)に対して高用量の副腎皮質ステロイドや二次免疫抑制薬を用いると、生存が損なわれる可能性が示されている。
非小細胞肺癌(NSCLC)では、十分な症例数を有する研究で検討されていない。
本研究は、ステージIV NSCLCでICI治療を受け、irAEに対して免疫抑制療法を受けた患者において、ステロイド投与量(最大投与量・累積投与量)および二次免疫抑制薬使用と生存転帰との関連を評価したものである。
方法
2015〜2022年に、一次または二次治療としてICIベースのレジメンを受けたステージIV NSCLC患者のうち、irAEに対して全身性の免疫抑制薬を投与された患者を、世界8か国17病院から後ろ向きに登録した。
ステロイドの最大投与量(1日の最大量)および累積投与量、二次免疫抑制薬使用と、
全生存(OS)、がん特異的生存(CSS)、無増悪生存(PFS)との関連をCox比例ハザードモデルで解析した。
結果
419例が解析対象。
339例(80.9%)はステロイドのみ、80例(19.1%)は免疫抑制薬も使用した。
ステロイド最大投与量が高いほど、
- OS不良[補正ハザード比(HRadj)1.63、95%信頼区間(CI)1.27–2.08:プレドニゾロン換算80 mg増加あたり]
- CSSも不良(HRadj 1.54、95%CI 1.13–2.08)
一方でPFSとの関連は認めなかった(HRadj 1.05、95%CI 0.75–1.48)。
ステロイド累積投与量および二次免疫抑制薬使用は、生存と関連しなかった。
結語
irAEに対する高いステロイド最大投与量は、ICIを受けるステージIV NSCLC患者の生存不良と関連した。
重篤なirAE治療には高用量ステロイドが必要となることが多いが、臨床医はirAEを速やかに制御する必要性と、高い最大投与量がもたらし得る不利益を比較すべきである。

感想です。
どんな結果だった?
研究デザインと対象
- 多施設・国際・後ろ向きコホート
- 対象:ステージIV NSCLC、ICI治療中にirAEで全身免疫抑制治療を要した患者
- 解析の起点:免疫抑制開始日からOS/CSS/PFSを測定(immortal time biasへの配慮)
アウトカム
- 免疫抑制開始後の中央値:OS 14.4か月、CSS 25.4か月、PFS 13.3か月
“最大投与量(peak dose)”は関連あり
一日あたりのステロイド最大投与量を <60 mg / 60–100 mg / >100 mg(プレドニゾロン換算)で比べると:
- OS:20.7か月 vs 15.4か月 vs 7.3か月(P<0.001)
- CSS:29.4か月 vs 30.8か月 vs 11.4か月(P=0.005)
- PFS:20.2か月 vs 12.6か月 vs 7.1か月(P=0.40:差なし)
さらにCox解析(多変量)では、最大投与量が高いほど
- OS悪化:HRadj 1.63(一日あたりの最大投与量80 mg増加あたり)
- CSS悪化:HRadj 1.54
- PFSは関連なし:HRadj 1.05
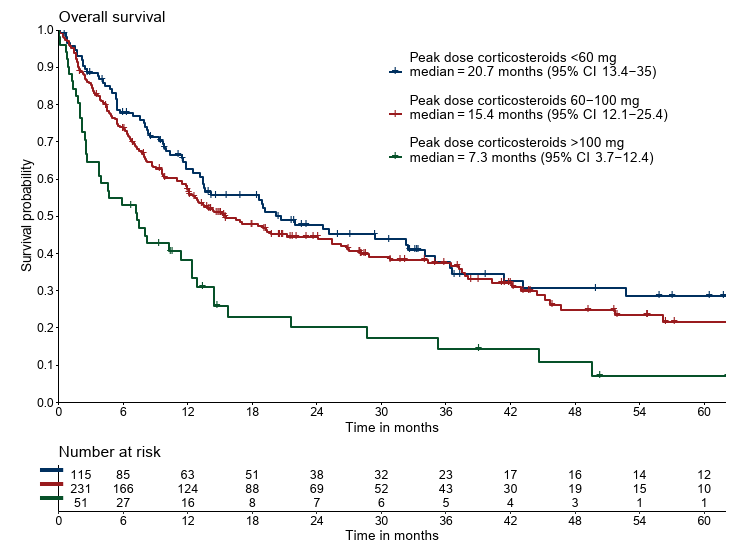
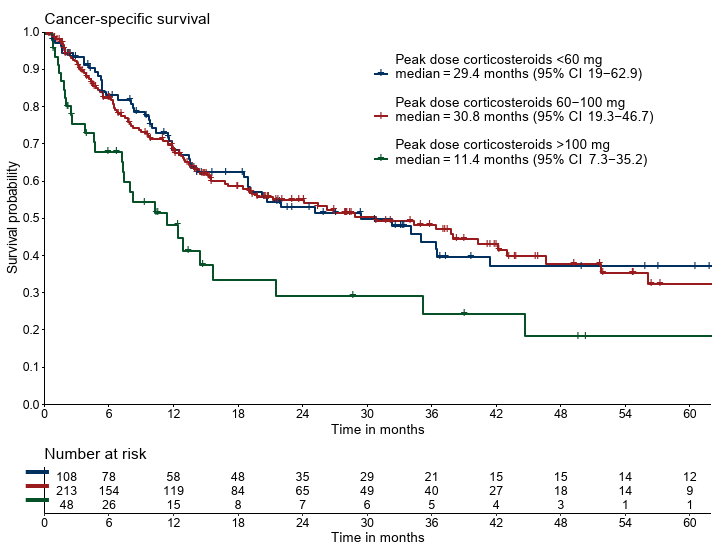
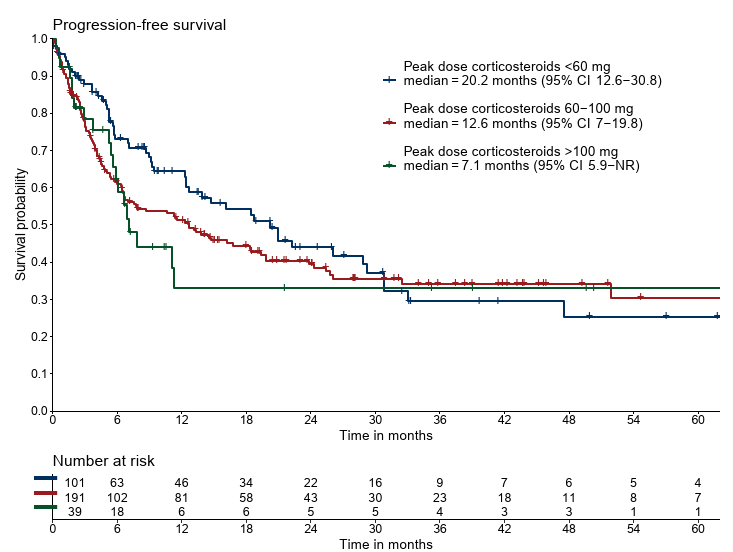
Figure 1. Overall survival, cancer-specific survival, and progression-free survival as assessed by Kaplan—Meier analyses, measured from start of immunosup-
pression, stratified for peak dose of corticosteroids.
“累積投与量(cumulative dose)”は関連なし
累積量(1000 mg増加あたり)は、OS/CSS/PFSいずれも有意な関連なし、さらにランドマーク解析でも同様でした。
二次免疫抑制薬も「有意な悪化なし」
ステロイド最大投与量などで調整した多変量解析で、二次免疫抑制薬はOS/CSS/PFSいずれも有意差なし。
ただし著者らは二次免疫抑制開始まで生き延びる必要がある(immortal time bias)を強く意識しており、時間依存解析では有利な傾向も消えた、としています。
論文解釈に注意するポイント
NSCLCの大規模コホートとして、高いステロイド最大投与量がOS/CSS不良と関連した点が重要です。
一方、累積投与量は関連しないため、免疫抑制の「総量」よりも「最大濃度(ピーク)」のほうが免疫機能に影響し得る、という薬力学的な議論も触れられています(ただし根拠は限定的)。
PFSで差が出なかった理由は不明で、実臨床の“医師判断の増悪”であること(中央判定なし)など、評価のばらつきが関与し得る、としていますね。
注意点 リミテーション
- 後ろ向き観察研究なので、交絡は避けられない(特に「重症irAEほど高用量になりやすい=適応によるバイアス」)。ただしGrade 3に限定しても結果は概ね一貫としています。
- 体重が約半数で欠損し、mg/kgでの厳密な解析が難しい。
- 併存症、過去の放射線治療歴、腫瘍量、前治療反応などが不明/欠損。
まとめ:臨床現場でどう活かす?
irAE治療のためのステロイド最大投与量は、生存不良と関連し得るので、必要性と不利益を天秤にかけよう。
具体例で考えると、
例えばGrade 3肺障害で呼吸不全が迫っている状況では、当然高用量ステロイドが必要な場面があります。
一方で、そうでもない症例に“とりあえず高いピーク”が習慣化してしまうと、抗腫瘍免疫を抑え込み得るかもしれません。
この研究は「累積量よりピーク量が問題かもしれない」という示唆なので、現場では次のような検討をする材料になります。
- 本当に1–2 mg/kg相当のステロイド最大量が必要か?(重症度・臓器障害の評価を丁寧に)
- 反応が悪いときに、漫然とピークを上げ続けるより、別戦略(早期二次免疫抑制?)を検討すべき?
このあたりのエビデンスも必要ですね。

<スマートフォンをご利用の皆さまへ>
他の記事をご覧になりたい場合は、画面下の「メニュー」「検索」「サイドバー」を使って、気になる話題を検索することもできますので、ぜひご活用ください。
<PCをご利用の皆さまへ>
他の記事をご覧になりたい場合は、画面上部のメニューバーや画面右側のサイドバーをご利用いただき、気になる話題をお探しください。

