Travis WD, et al. An official American Thoracic Society/European Respiratory Society statement: update of the international multidisciplinary classification of the idiopathic interstitial pneumonias. Am. J. Respir. Crit. Care Med. 2013; 188: 733–748.
関連記事:HRCTと病理学的UIP
関連記事:蜂巣肺について
はじめに
特発性間質性肺炎(IIPs)のひとつである「非特異的間質性肺炎(NSIP)」について解説します。
最初は“その他”扱いだったNSIP
NSIPとは「Non-Specific Interstitial Pneumonia」の略で、日本語では「非特異的間質性肺炎」と訳されます。
もともと、「どう分類すればいいのか分からない肺の病理像」に対して便宜的につけられていた名前でした。
要するに、「特定の型には当てはまらないけど、間質性肺炎っぽい病理像だなあ……」というような“その他枠”の存在だったのです。
時代が進み、ひとつの病気として認められた
そんなNSIPですが、過去20年ほどで研究が進み、「これはただのその他ではなく、特徴のある立派な病気だ」と認識されるようになりました。
さらに、NSIPの中でも明らかな原因が見つからないものは「特発性NSIP(iNSIP)」と呼ばれ、IIPsの一つとして分類されるようになります。
ただし、このiNSIPという診断も最初から認められていたわけではありません。
というのも、NSIPは膠原病(リウマチなど)に伴ってよく見られる病理像でもあり、「本当に特発性といえるのか?」という疑問があったためです。
2013年、正式な病気として仲間入り
2002年には、アメリカ胸部学会とヨーロッパ呼吸器学会がiNSIPを“暫定的な疾患”として一時的に認めました。
そして研究が進み、2008年には専門家グループによる詳細な報告が出され、ついに2013年、iNSIPは正式な特発性間質性肺炎として認められることになりました。それ以降2025年現在まで、疾患概念のアップデートはまだありません。
「特発性NSIP」の診断はなぜ難しいのか?〜除外診断と自己免疫の関係〜
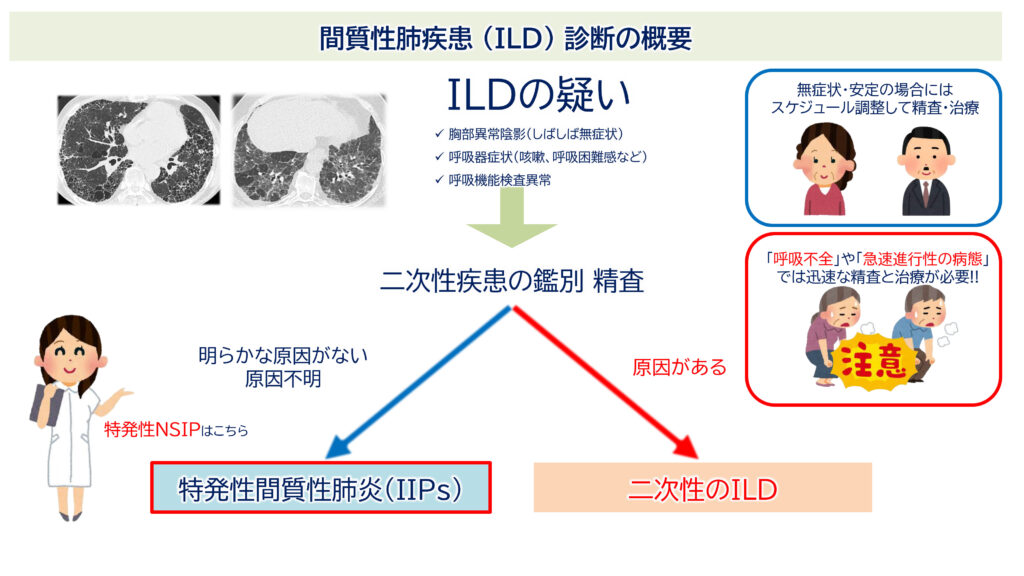
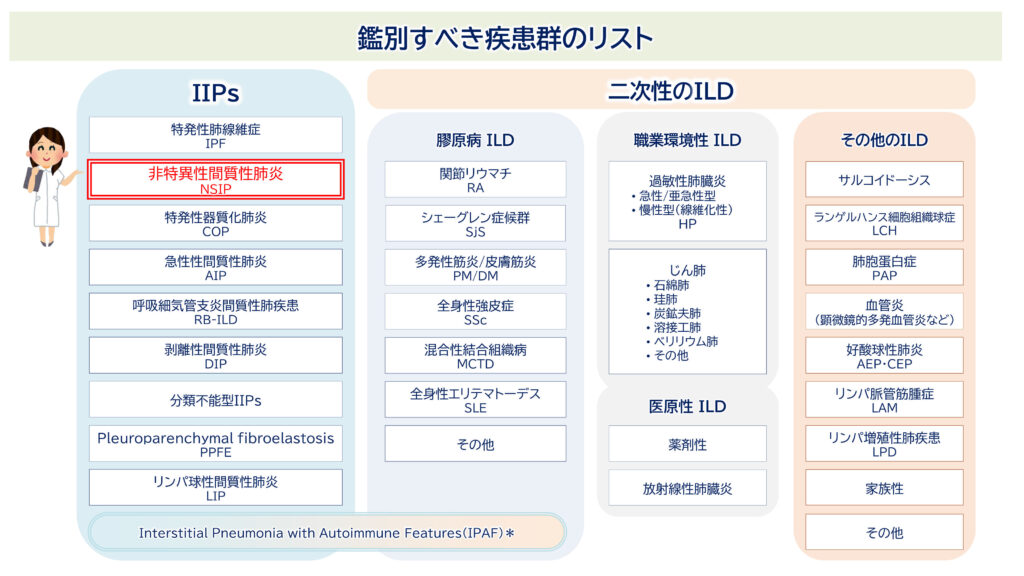
NSIPの診断は一筋縄ではいきません。
まず最も重要な点として、現時点のガイドラインにおいて、特発性NSIPの確定診断には外科的肺生検(SLB)を含む病理学的診断が必須とされています。
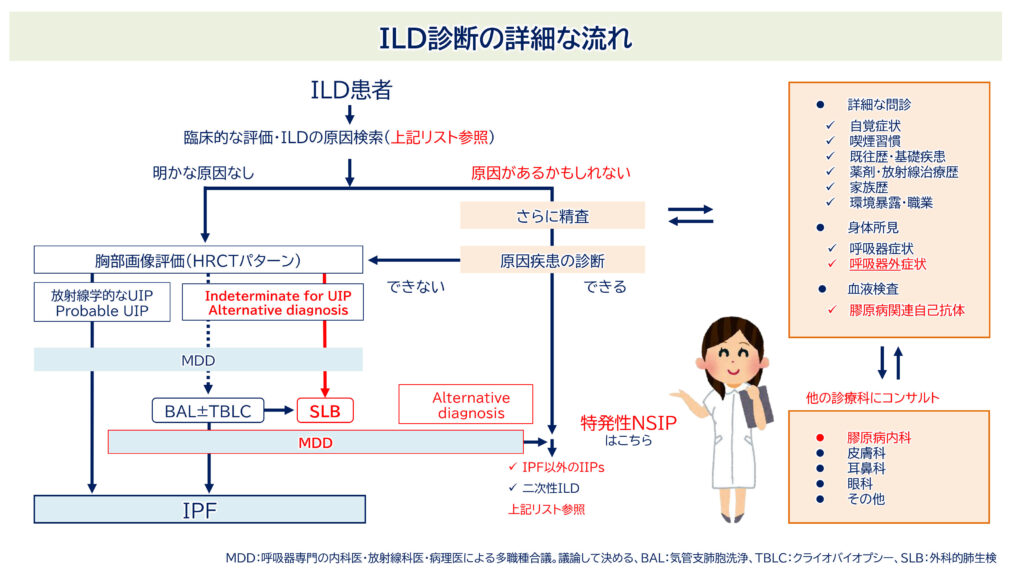
地方会などで「胸部HRCTのみでNSIPと診断した」と発表されるケースをしばしば目にしますが、これは現行の診断基準に照らすと正確ではありません。注意しましょう。
また後述しますが、IPFにおける典型的なHRCT所見であるUIPパターンとは異なり、NSIPにおけるHRCTパターンは現時点で明確な定義がなく、十分に確立されているとは言えません。そのため、放射線科医間でも読影結果にばらつきが生じやすく、再現性が高いとはいえないのが現状です。
NSIPと間違えやすい病気たち
まず知っておきたいのは、「NSIPっぽく見えるけど、実は別の病気だった」というケースが非常に多いということです。
初期診断の過程で、原因不明の間質性肺炎、すなわちIIPsと判断された場合、まず典型的なUIP(usual interstitial pneumonia)パターンを示すIPFはNSIPと明確に区別できます。
しかし、初期のIPFや非典型的なIPFでは、画像や病理所見が進行したNSIPと類似することがあり、両者の鑑別がしばしば必要になります。
UIPとNSIPでは予後に大きな違いがあり、UIPの方が予後不良であるため、鑑別を誤ると治療方針が根本的に異なってしまいます。
IPFでは抗線維化薬(ピルフェニドン、ニンテダニブ)が用いられますが、慢性期におけるステロイドや免疫抑制薬の使用はむしろ有害とされています。
一方、NSIPはステロイドや免疫抑制薬による治療が基本であり、進行例ではPF-ILDとしてニンテダニブの投与が考慮されます。このように、両者では治療戦略が大きく異なります。
さらに、NSIPと鑑別すべき特発性間質性肺炎には、COP(特発性器質化肺炎)や喫煙関連ILD(DIPおよびRB-ILD)なども含まれます。
「NSIPパターン」≠「iNSIP」
ここで少し用語を整理しておきましょう。
肺生検でNSIPに一致する病理が得られたとき、それは「NSIPパターン」と呼ばれます。これは単なる病理所見であり、必ずしもiNSIPとは限りません。
病理学的なNSIPパターンは、HPやUIP、CTD-ILD、薬剤性肺障害などでも出現します。つまり、「NSIPパターンです」と病理医に言われたら、それを臨床所見・画像所見と統合して、他の疾患を除外していく必要があります。
このときに行うのが、多職種によるディスカッション(MDD:multidisciplinary discussion)です。呼吸器内科医、放射線科医、病理医が集まって総合的に診断を行うのが、NSIP診断の“王道”です。
本当に特発性?自己免疫性疾患の可能性
診断において特に重要なのが、自己免疫性疾患(膠原病)との関連です。
実際、NSIPと診断された患者の中には、後になって膠原病と診断されるケースが少なくありません。関連する疾患としては、多発性筋炎/皮膚筋炎、全身性強皮症、関節リウマチ、シェーグレン症候群などが代表的です。
さらに、「未分類型膠原病(UCTD:undifferentiated connective tissue disease)」という概念もあります。これは、膠原病を疑わせる症状や自己抗体の存在はあるものの、既存の診断基準を満たさない状態を指します。NSIPの患者の中には、このUCTDに該当する症例が多く、「すべてのiNSIPは実は自己免疫疾患に由来しているのではないか」という意見もあるほどです。
若年~中年女性では膠原病発症に注意が必要
NSIPと診断された後、9〜33%の人が後に膠原病を発症すると言われています。特に若年~中年女性でそのリスクが高い可能性が示唆されています。
そのため、iNSIPと診断された方には、診断後も定期的な膠原病のスクリーニング(問診や血液検査)を行うことがすすめられています。
NSIPの画像診断:HRCTで何がわかる?何がわからない?
胸部X線
NSIPでは、胸部X線上、両下肺野を中心としたすりガラス影や浸潤影が見られることが多く、これらは比較的対称性を持っています。病状が進行すると、両下肺野の容積減少が目立つようになるのも特徴です。
一方で、初期の段階では両上肺野に目立った陰影が見られないことが多く、診断を難しくさせる要因となります。とくにすりガラス影が淡い場合には、X線所見としてははっきりとした異常が捉えにくく、「なんとなく下肺野が縮んでいるように見える」といった印象にとどまることもあります。
HRCT
NSIPにおけるHRCT所見としては、以下のような特徴が知られています(ATS 2008年の報告より):
- 下肺優位の病変が大多数(92%)
- びまん性または末梢優位な分布
- 網状影(reticular abnormality)(87%)
- 牽引性気管支拡張(82%)
- 肺葉の容積減少(77%)
- すりガラス影(44%)
- 胸膜直下の保たれた部分(subpleural sparing)(21%)
この「subpleural sparing」はNSIPを示唆する特徴ですが、これだけでNSIPと確定できる所見ではありませんし、頻度も決して多いわけではありません。
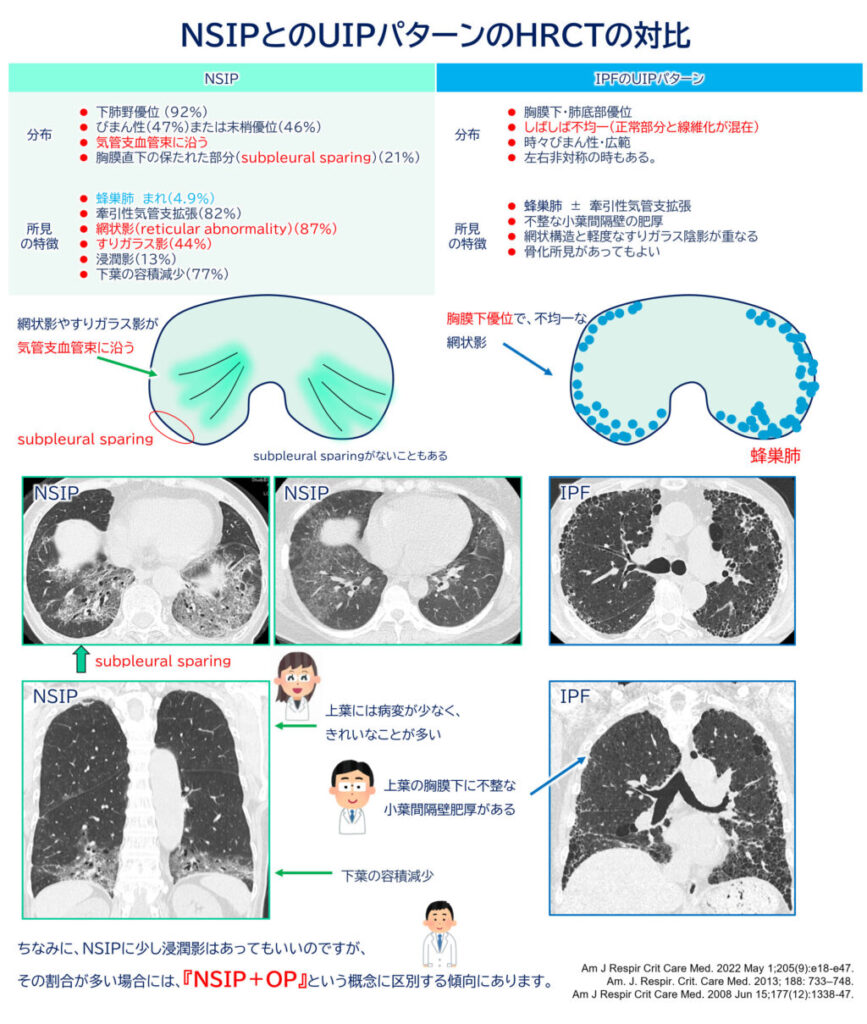
NSIP vs. UIP:見分けはつくのか?
NSIPの鑑別で最も重要なのがUIPです。
UIPはIPFの代表的な病理・HRCTパターンで、予後や治療方針がNSIPとは大きく異なるため、正確な診断が不可欠です。
UIPは以下のようなHRCT所見で診断されることがあります:
- 下肺・胸膜直下優位の網状影
- 蜂巣肺(honeycombing)と牽引性気管支拡張
- 不均一な所見
- すりガラス影が少ない
特に「蜂巣肺」はUIPを支持する所見として非常に重要ですが、NSIPでもごく稀に蜂巣肺が見られることがあります(4.9%)。このため、蜂巣肺があるからといって即UIPと判断するのは早計です。
また、HRCT上蜂巣肺が見られなくてもUIPの可能性があるため、画像のみでの除外はできません。外科的肺生検やクライオ生検が必要となることがあります。
NSIPに合致しない所見があれば要注意
NSIPと考えていたとしても、HRCTで以下のような所見が見られた場合は他の疾患を疑う必要があります:
- 上肺優位の小葉中心性結節やモザイクパターン → 過敏性肺炎(HP)
- 肺の一部に強いすりガラス陰影やコンソリデーション、対称性ではない → 特発性器質化肺炎(COP)
画像だけでは決まらない
ここまでお読みいただいてお気づきかもしれませんが、NSIPはHRCTだけでは確定診断できません。むしろ、病理、臨床経過、自己免疫評価などを含めたMDDが必須となります。
NSIPかUIPかの鑑別は、患者さんの予後や治療法に直結する重要な分岐点です。画像は「ヒント」にはなりますが、答えではないという視点を持つことが大切です。
NSIPの病理診断:組織を見なければ始まらない?
組織診が必要
NSIPを疑ったとき、画像でUIP(特発性肺線維症の典型パターン)や過敏性肺炎(HP)、薬剤性肺障害、膠原病関連ILDなどを除外し、それでも原因がはっきりしない場合には、組織を見てNSIPの病理パターンかどうかを確認することが不可欠です。
一般的にはSLBが行われますが、最近では気管支鏡によるクライオ生検も注目されており、より低侵襲でNSIP診断に用いられることがあります。
NSIPの典型的な病理所見
NSIPの特徴的な病理像は以下の通りです:
- 時間的均一性(temporal uniformity):組織全体で炎症や線維化の進行度がそろっている
- 肺胞壁の慢性炎症や線維化
- リンパ球・形質細胞の浸潤
- 線維化があれば、線維芽細胞は少なく、成熟したコラーゲン束が主体
これは、UIPのように「炎症+線維化+蜂巣肺」がモザイク状に混在する時間的な不均一性とは大きく異なります。
NSIPはさらに病理学的に次の2タイプに分類されます:
- Cellular型(炎症が主体)
- Fibrosing型(線維化が主体)←約80%はこちらに該当
他に以下のような所見も時に見られますが、UIPほど顕著ではありません:
- Fibroblastic foci (線維芽細胞巣)(21%)
- Organizing pneumonia (器質化肺炎)(52%)
- リンパ濾胞(57%)
- 肺胞内マクロファージの斑状な沈着
注意!病理診断にも限界がある
病理診断にもいくつかの落とし穴があります:
- 病理医間の診断の一致率はそれほど高くない
→ SLBを使ってもkappa値は0.26~0.49と低め。複数葉からのサンプルでやや向上。 - 一つの肺葉だけで診断すると見落としの危険あり
→ 1葉でNSIPでも、他の葉にUIP所見が存在することがある。 - NSIPと思っていたら、実は他の病態とのオーバーラップだった
→ 近年ではNSIP/UIP、NSIP/過敏性肺炎、NSIP/器質化肺炎などの「オーバーラップパターン」も提唱されています。
→ こうした病理像は、それぞれの臨床背景(膠原病や曝露歴)と整合することが多いです。
本当に「特発性」と言えるのか?
NSIPの病理診断がついたら、次にすべきなのはもう一度、原因を見落としていないか確認することです。
- 隠れた膠原病(未分類型含む)
- 知られていない抗原への曝露(鳥、カビ、職場環境など)
- 薬剤歴(抗リウマチ薬、抗がん剤、生物学的製剤など)
NSIPの予後と治療:どう経過する?どう治す?
予後:IPFより良好、でも油断は禁物
NSIPは、IPFと比較して全体的に予後が良好とされています。
たとえば、2008年のATS報告では、特発性NSIP(iNSIP)の5年生存率は82%、10年生存率は73%とされています。
一方で、IPFでは5年生存率が20〜40%、10年生存率は約15%とされており、両者の間には明らかな差があります。
しかし、ここで重要なのは、NSIPとIPFでは患者の年齢層が大きく異なるという点です。NSIPは40〜60歳代の比較的若い層に多いのに対し、IPFは60〜80歳代の高齢者に多い傾向があります。
そのため、「NSIPは10年生存率が高いから予後良好」と単純に評価することは適切ではありません。若年〜中年層を中心とするNSIPでは、むしろ20年、30年といった長期的な生存率が重要な指標となるべきです。
将来的には、こうした長期予後に関する視点からの解析やエビデンスの蓄積が求められます。
病理タイプによっても予後が違う
NSIPには大きく分けて2つの病理タイプがあります:
- Cellular型(炎症優位)
- Fibrosing型(線維化優位)
一般的に、Cellular型の方が予後が良いとされています。ある研究では、Cellular型では10年生存率100%、Fibrosing型では35%と大きな差が見られました。
とはいえ、Fibrosing型でもIPFに比べれば良好な予後であり、病理タイプは重要な初期情報となります。
治療
NSIPの自然経過(未治療時の予後)については、まだ十分に明らかになっておらず、ランダム化比較試験も存在しません。それでも、ステロイドや免疫抑制薬によって症状や肺機能の改善・安定が期待できるケースが多く、現時点では治療が推奨されています。
軽症・無症状例では「経過観察」も選択肢
症状が軽度で病勢が安定している場合には、定期的な観察(経過観察)によって治療を見送ることも可能です。不要な治療による副作用リスクを避けるためにも、慎重な判断が求められます。
ステロイド
治療を開始する場合、プレドニゾロン 0.5~1 mg/kg/day または40~60 mg/日(体重非依存)で開始されるのが一般的です。
免疫抑制薬の併用・代替
副作用対策や再燃防止のため、以下の免疫抑制薬が併用または代替薬として使用されます:
- アザチオプリン
- ミコフェノール酸モフェチル
- タクロリムス
- シクロホスファミド
- シクロスポリン
- リツキシマブ(未分類型膠原病のNSIPで報告あり)
進行例では抗線維化薬や肺移植も視野に
上記の治療でも病状が進行する場合には、PF-ILD(進行性線維化を伴うILD)として、ニンテダニブの併用が検討されます。
また、NSIPは若年~中年層に多い疾患であることから、肺移植も早期に選択肢に含めるべきです。
治療方針の詳細については、『特発性間質性肺炎 診断と治療の手引き2022(改訂第4版)』も参考にしましょう。
【まとめ】NSIP診療の重要ポイント
- NSIPはIPFより予後が良好だが、予後不良な経過をたどる例もある。
- HRCTは診断の手がかりになりますが、確定診断には組織診とMDDが必須。
- 「NSIPパターン=NSIP確定診断」ではないことに注意。
- 若年~中年女性の頻度が多く、とくに膠原病の発症に注意。
- 治療の中心はステロイド ± 免疫抑制薬ですが、確立したエビデンスはない。PF-ILDの場合にはニンテダニブ追加も。
- 若年発症の場合には、将来的に肺移植も?

