Radiologic Pattern of Fibrosis in Combined Pulmonary Fibrosis and Emphysema: Impact on Disease Trajectories and Prognostic Outcomes. Min Seon Kim, et al. Radiology 2026
CPFEでも、CTの線維化パターンは予後に影響するのでしょうか。
もし影響するなら、やはりUIPパターンが最も悪いのではないか――そう考えたことはありませんか?
今回紹介するRadiologyの論文では、CPFE 236例を対象に線維化パターンと予後の関係を検証しています。
その結果、生存を左右していたのはパターンそのものではなく、ベースラインの線維化量と肺癌・急性増悪という臨床イベントであることが示されました。
Published by the Radiological Society of North America under a CC BY 4.0 license.
はじめに

CPFEは「上肺野優位の肺気腫」と「下肺野優位の線維化」が同時にある病態として知られています。
特徴として、FVCが比較的保たれるわりに、Dlcoが低下しやすく、FVCだけでは進行評価が難しいと言われています。
さらに、肺高血圧や肺癌が多いこともCPFEを特徴づける重要な点です。

近年、CPFEの研究定義(ATS/ERS/JRS/ALAT)が提案され、「肺気腫が総肺容量の≥5%」などを満たすこと、そして画像・病理パターンを詳述することが推奨されています。
ただ、線維化の“画像パターン”が、病勢(線維化や肺気腫の進み方)や予後にどう影響するのかは未解明でした。
そこで本研究は、CPFEを線維化パターン(UIP/NSIP/SRIF/DIPなど)で分けたとき、進行や転帰が違うのかを検討しています。
背景と目的
肺線維症合併肺気腫(combined pulmonary fibrosis and emphysema:CPFE)は画像パターンが多様であるが、それが病勢進行や臨床転帰に与える影響は十分に理解されていない。
本研究の目的は、CPFE患者において、異なる線維化パターンが病勢および転帰に与える影響を評価することである。
方法
本後ろ向き研究は、2011年1月から2021年12月の間に高分解能CTを施行した患者を対象とした。
CPFEは、総肺容量の少なくとも5%を占める(サブタイプを問わない)肺気腫と、CTでの線維化所見の併存として定義し、追跡データが利用可能な患者を含めた。
画像上の線維化パターンは、通常型間質性肺炎(usual interstitial pneumonia:UIP)および/またはprobable UIP(放射線学的UIP)と、それ以外(非特異性間質性肺炎[NSIP]、喫煙関連間質性線維化[SRIF]、剥離性間質性肺炎[DIP])に分類した。
深層学習に基づく定量化を用いて肺気腫と線維化の範囲を評価した。
縦断的転帰はCox比例ハザードモデルで解析した。
結果
CPFE患者236例を含めた(平均年齢65歳±7.8[SD]、男性232例)。
236例中、UIP 99例(41.9%)、NSIP 73例(30.9%)、SRIF 48例(20.3%)、DIP 14例(5.93%)、分類不能2例(0.85%)であった。
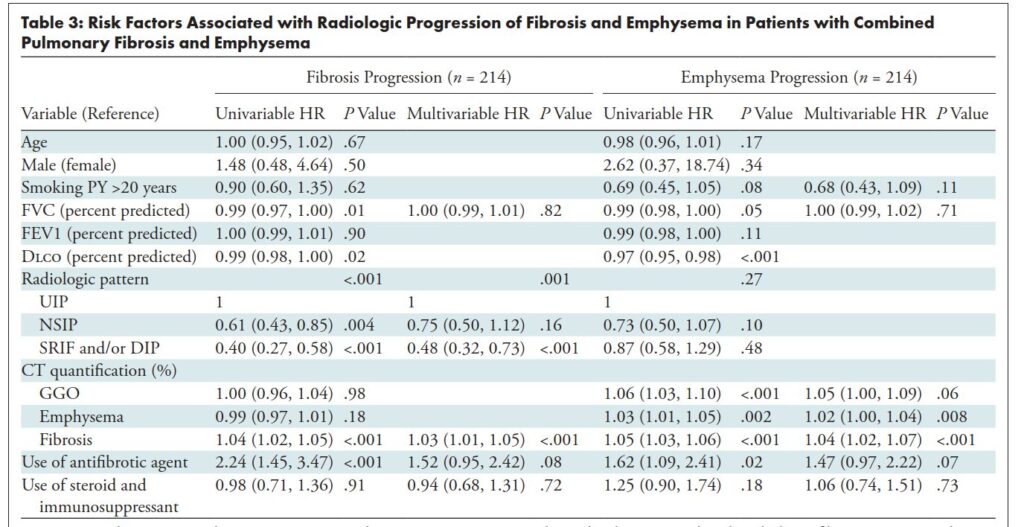
線維化パターンは線維化の進行速度と関連し、UIPが最も速く(中央値1.2年)、次いでNSIP(中央値2.1年)、SRIFまたはDIPが最も遅かった(中央値3.0年;P<.001)。
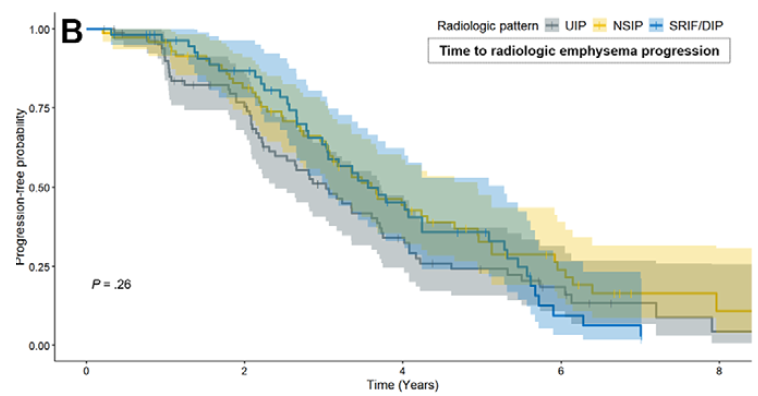
しかし、線維化パターンは、肺気腫の進行(単変量P=.27)、肺移植なし生存(多変量P=.55)、時間依存性肺癌(多変量P=.65)、急性増悪(多変量P=.64)と有意な関連を示さなかった。
ベースラインの線維化範囲が大きいこと(調整HR 1.04;95%CI 1.02–1.06)、肺癌(調整HR 3.90;95%CI 2.55–5.96)、急性増悪(調整HR 4.31;95%CI 2.68–6.94)は予後不良と関連した。
結語
CPFE患者では、画像上の線維化パターンは線維化の進行速度と関連する一方で、生存は主としてベースラインの線維化範囲と、肺癌の発症を含む有害な臨床イベントによって規定される。

感想です。
どんな研究でどんな結果だったか?
研究デザインと分類
- 単施設・後ろ向き研究で、2011–2021年にHRCTを受けたCPFEを抽出。
- CPFE定義は「CTで線維化+肺気腫(亜型不問)が総肺容量の≥5%」
- 線維化パターンはUIP、NSIP、SRIF、DIP、分類不能に分類し、SRIFとDIPは解析上まとめています(SRIF/DIP)。
- 肺気腫・線維化の範囲は深層学習ベースの全肺定量(線維化=reticulation+honeycombing)で評価しています。
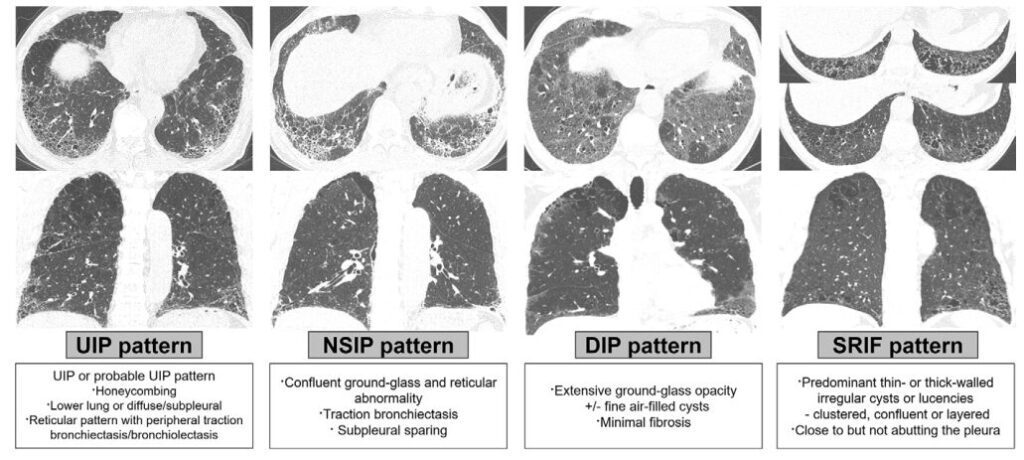
図2
患者背景(全体)
- 236例、平均65歳、男性98.3%。→女性ほとんどいない。
- 喫煙:現在50.0%、過去49.2%、非喫煙0.85%、pack-years中央値40。
- 肺癌 28.8%(ベースライン7.2%、追跡中21.6%)、急性増悪28.8%、死亡57.6%。
線維化パターンの分布
UIP 41.9%、NSIP 30.9%、SRIF 20.3%、DIP 5.9%、分類不能0.85%。
重要アウトカム①:線維化進行スピード(速い順)
線維化進行までの中央値
- UIP:1.2年
- NSIP:2.1年
- SRIF/DIP:3.0年(群間差あり)
さらに、多変量ではUIPと比べ、SRIF/DIPは線維化進行ハザードが低い(調整HR 0.48)
一方、NSIPはUIPとの有意差なし。
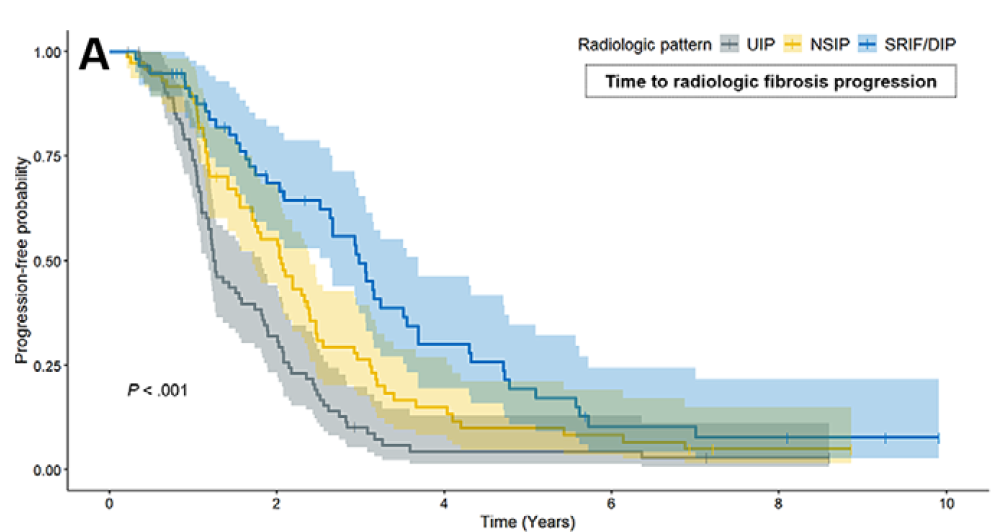
図4A
「線維化進行」:UIPが早く落ちる、NSIPが中間、SRIF/DIPが最もゆっくり。
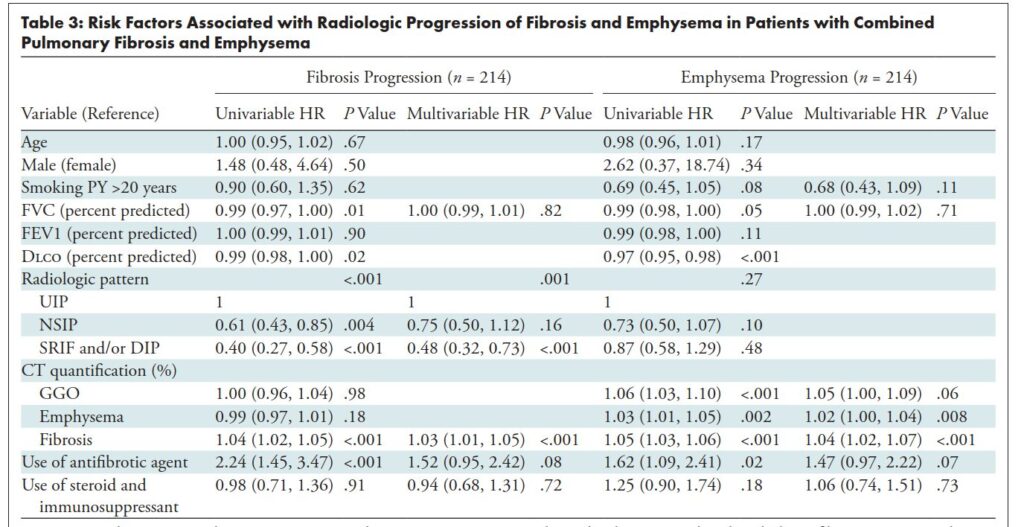
重要アウトカム②:肺気腫進行
線維化パターンは肺気腫進行と関連しない。(図4B)
肺気腫進行は、ベースラインの肺気腫範囲・線維化範囲が大きいほど速い(多変量)。
重要アウトカム③:生存(肺移植なし生存:TFS)
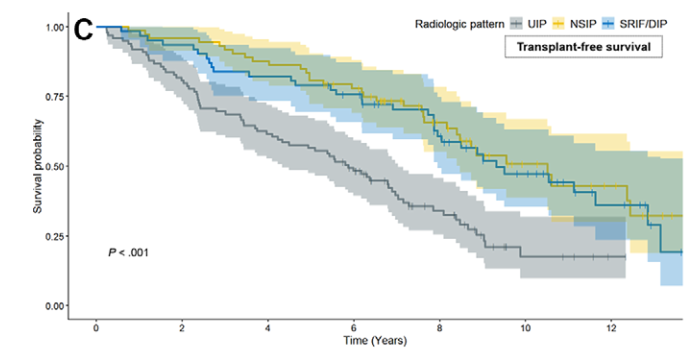
図4Cで、未調整ではUIPが悪そうに見える一方、多変量では「線維化パターンそのもの」は独立した予後因子になりませんでした(P=0.55)。
代わりに、予後を規定したのは以下です:
- ベースライン線維化範囲(調整HR 1.04)
- 肺癌(時間依存共変量;調整HR 3.90)
- 急性増悪(時間依存共変量;調整HR 4.31)
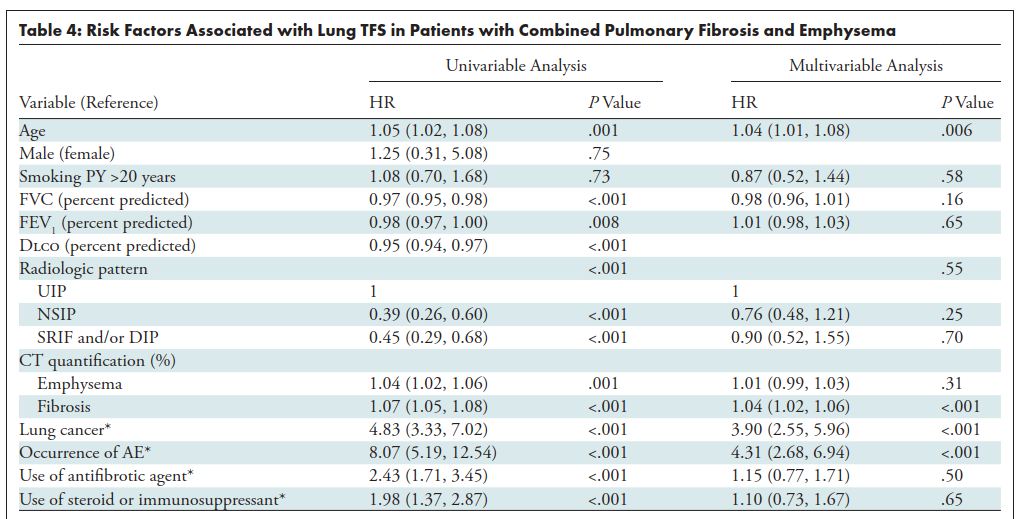
重要アウトカム④:肺癌・急性増悪(AE)
- 肺癌は追跡中に一定数発生するが、線維化パターンとは独立関連がない(多変量P=0.65)。
- AEも同様に、調整後は線維化パターンと独立関連しない(多変量P=0.64)。
結果をどう解釈するか?
まとめると、
- 画像の線維化パターン、例えばUIPパターンは“線維化の進行”に関係する。
- しかし、予後はパターンではなく、ベースラインの線維化量と肺癌・急性増悪などのイベントに左右される。
- 気腫の総量は予後と有意な関連なし。
なぜ線維化パターンが独立した予後因子にならなかったのかについて、本文では主に次の理由が考察されています。
- 線維化パターンはベースラインの線維化量(重症度)と強く相関している可能性があること(多重共線性や媒介の可能性?)
- 肺癌やAEといった“下流イベント”の影響が大きいのでは?
- パターン分類の観察者一致が中等度であること(κ=0.45)→つまり、気腫がある分、パターン分類が難しい可能性。
NSIPは病理との一致が相対的に低く、時間経過でUIP様に見えてくるケースもある(NSIP/SRIF/DIPからUIP様へ移行)ので、そもそも分類の難しい可能も考えられますね。
注意点 リミテーション
- 単施設・後ろ向き。
- 併存疾患や未測定因子の交絡(肺高血圧など。右心カテ情報が限られる)の欠損
- 画像分類の一致が中等度、画像—病理不一致あり。
- 抗線維化薬など治療の影響。
- CPFEでは肺気腫・蜂巣肺・非気腫性嚢胞変化が混在し、定量画像の精度にも限界がある
まとめ:臨床現場でどう活かす?
- CPFEでは、線維化パターン、特にUIPパターンが線維化進行と関連する。
- しかし、予後に関連するのはパターンではなく、線維化の総量。
- CPFEでは“肺癌と急性増悪”に注意する。

<スマートフォンをご利用の皆さまへ>
他の記事をご覧になりたい場合は、画面下の「メニュー」「検索」「サイドバー」を使って、気になる話題を検索することもできますので、ぜひご活用ください。
<PCをご利用の皆さまへ>
他の記事をご覧になりたい場合は、画面上部のメニューバーや画面右側のサイドバーをご利用いただき、気になる話題をお探しください。

